Tout est dans le choix du moment : quand envisager les BPFc ?
Les bonnes pratiques de fabrication (BPF) sont au cœur de la fabrication des médicaments, car elles permettent de produire des produits chimiques et d'autres matières premières conformément à des contrôles et à des systèmes de qualité spécifiques. Malgré l'impact significatif des BPF sur la qualité et la cohérence des médicaments, une étude récente1 indique que seulement la moitié environ des développeurs biopharmaceutiques utilisent des produits chimiques conformes aux BPF dans les essais cliniques de première phase.
Étant donné le développement rapide de produits biologiques complexes et la pression constante pour passer à la production, les conséquences de l'introduction d'une matière première non conforme peuvent être catastrophiques.
Souvent, des matières premières à usage exclusif de la recherche (RUO) sont utilisées au cours des premières étapes. Les matières RUO ne sont pas soumises aux mêmes contrôles rigoureux de fabrication et de qualité que les matières premières cGMP. C'est pourquoi les variables qui pourraient être introduites par inadvertance par l'utilisation de produits chimiques RUO pourraient entraîner des retouches et le rejet potentiel de lots entiers de produits pharmaceutiques finis.
Toutefois, en utilisant des matières premières conformes aux BPF plus tôt dans le processus de développement des médicaments, les fabricants peuvent minimiser ces risques et accélérer leurs étapes de développement.
Une transition en douceur
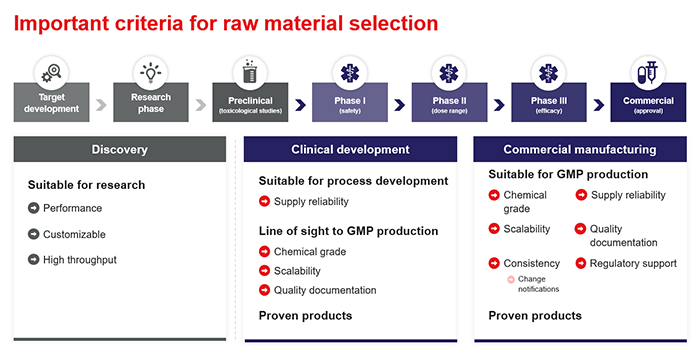
Les produits chimiques fabriqués selon les normes rigoureuses des BPF comportent une attente de haute qualité. Ils sont vendus avec une certification complète attestant de la conformité de chaque lot fabriqué aux normes publiées. Le Conseil international d'harmonisation (CIH) et de nombreux autres organismes de réglementation stipulent généralement que les matériaux et les fournisseurs fabriqués selon les BPF doivent être introduits après l'achèvement des essais précliniques.
Toutefois, l'adoption précoce de produits chimiques conformes aux BPF peut contribuer à faciliter la transition entre la phase de recherche et la production clinique. Cela permet de simuler plus fidèlement les conditions réelles dans lesquelles le médicament sera utilisé lors des premiers essais sur l'homme (FIH). D'un autre côté, le changement de qualité chimique, de spécification ou de fournisseur lors du passage aux essais FIH nécessite une validation et une qualification supplémentaires, ce qui demande beaucoup de temps et de ressources. La planification de ces normes de conformité et de qualité à un stade précoce du processus peut grandement contribuer à minimiser les coûts et la complexité.
S'attendre à l'inattendu
La concurrence pour les matières premières vitales a atteint des niveaux sans précédent. Bien que les perturbations résultant des pics de demande puissent certainement exacerber ces problèmes, les pénuries constituent un défi depuis un certain temps. L'évaluation de la disponibilité de l'offre et de la qualité de vos produits chimiques, même pour le RUO, et l'établissement de relations avec des fournisseurs de confiance peuvent contribuer grandement à atténuer les perturbations de l'approvisionnement qui peuvent survenir.
Dans le même ordre d'idées, une fois que vos données permettent de passer aux essais cliniques, il est utile de rechercher des produits chimiques de meilleure qualité auprès de vos fournisseurs. Ce "travail préparatoire" peut faciliter les étapes ultérieures, car la nécessité d'agir rapidement implique de prendre le temps d'organiser les matériaux et de documenter les processus, ainsi que de planifier la transition. De meilleurs intrants permettent d'obtenir de meilleurs résultats.
Planifier pour réussir
Un fournisseur de qualité vous aidera à réduire les risques et à éliminer le gaspillage et les inefficacités dans l'approvisionnement de vos produits chimiques. En intégrant plus rapidement les BPF dans votre flux de travail, vos équipes pourront se concentrer sur ce qu'elles font le mieux : créer de nouveaux médicaments susceptibles de sauver des vies. Un tel fournisseur disposera d'une équipe dédiée, expérimentée dans l'approvisionnement en produits chimiques cGMP, pour vous soutenir depuis les premiers stades cliniques jusqu'à la commercialisation, et sera capable d'apporter une visibilité hors du commun à votre chaîne d'approvisionnement et de la transparence à votre planification de production.
Thermo Fisher Scientific offre une distribution cGMP et une expérience de la chaîne d'approvisionnement pour aider les clients à éviter de nombreux maux de tête liés à la mise à l'échelle. Grâce à nos relations mondiales avec les fabricants et les fournisseurs, nos services permettent non seulement de rationaliser les processus de pré-production, mais aussi de maintenir la production en conformité avec les normes de qualité et de réglementation, ce qui vous aide à aborder chaque étape de votre flux de travail de biofabrication en toute sérénité.
Références
1. Dérivé des rapports et études de Thermo Scientific Production Chemicals and Services, www.thermofisher.com/us/en/home/life-science/bioproduction/production-chemicals-services.html

